Biologie des hépatites
I. Exploration biochimique
Les paramètres utiles à étudier sont :
- La bilirubine totale : inférieure à 17 micromol/L chez le sujet normal, supérieure à 50 micromol/L au cours des ictères et comprise entre 30 et 50 micro- mol/L en cas de subictère.
- Les transaminases sériques : aspartate aminotransférase (ASAT) et alanine aminotransférase (ALAT).
Leur taux s’élève dans les hépatites :
à 10 fois la normale dans les hépatites aiguës ;
< à 10 fois la normale dans les hépatites chroniques.
Le taux de prothrombine (temps de Quick) et éventuellement le dosage du facteur V, très diminués dans les hépatites fulminantes.
L’albumine.
La numération formule sanguine, qui peut mettre en évidence une anémie, une thrombopénie et/ou une neutropénie avec éventuelle activation lymphocytaire. Le frottis sanguin permet d’éliminer un paludisme à la phase aiguë de la maladie.
II. Exploration virologique
| Rappel sur les méthodes de détection Le diagnostic biologique des différentes étapes de la maladie est effectué par la détection des marqueurs virologiques de l’infection. Il s’agit soit de méthodes immuno-enzymatiques de type ELISA (Enzyme Linked Immuno-Sorbent Assay) réalisables dans des laboratoires de routine, soit de techniques moléculaires, détectant et/ou quantifiant la séquence de l’ADN ou l’ARN du virus (charge virale), qui relèvent de laboratoires spécialisés. Méthodes ELISA Elles reposent sur l'utilisation d'un support solide recouvert soit d'antigènes viraux pour la détection des anticorps, soit d'anticorps monoclonaux pour la détection des antigènes. Le sérum du patient est mis au contact du support ainsi revêtu. Un complexe antigène-anticorps se forme alors. La révélation de ce complexe est effectuée par la fixation d'une enzyme transformant un substrat spécifique en composé coloré ou émettant un signal dont l’intensité est ensuite mesurée. De nombreux réactifs, aux performances sensiblement équivalentes, pouvant être utilisés sur des automates ou de façon manuelle (avec toutefois un minimum d'équipement et beaucoup de soin), sont aujourd'hui disponibles pour la détection des marqueurs du VHB. Les techniques sont décrites de façon précise dans chaque type de coffret. Tests de diagnostic rapide (TDR) Plusieurs tests rapides sont maintenant disponibles (Vikia Ag HBs, Immuno Comb HCV…). Faciles à utiliser, ils permettent un diagnostic en moins d’une heure à partir du sang ou de la salive, de sensibilité et spécificité satisfaisante. leur coût reste encore assez élevé. Tests moléculaires La détection/quantification de l'ADN/ARN des virus des hépatites est le meilleur marqueur de réplication virale. Elle fait appel à des techniques d’amplification génique de type Polymerase Chain Reaction (PCR). Elle est utilisée pour poser une indication thérapeutique et pour le suivi du traitement. Elle est également utilisée en transfusion pour rechercher, après un don de sang, une contamination éven tuelle d’un PSL (produit sanguin labile) par l’HCV et, selon les pays, l’HVB. Il s’agit du DGV (diagnostic génomique viral). |
1. Hépatite A
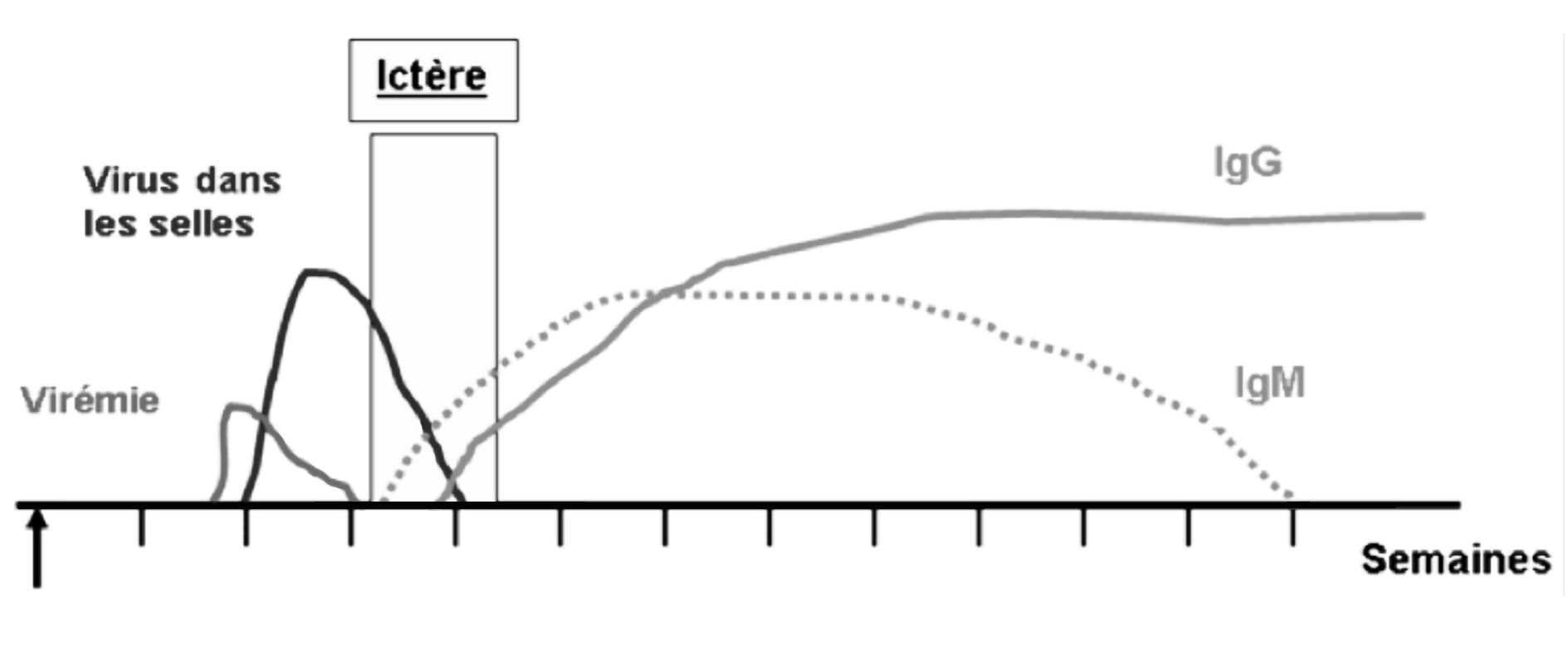
Les anticorps dirigés contre le virus de l’hépatite A apparaissent quelques jours avant le début des symptômes, ce sont des IgM et des IgG anti VHA. Les IgM atteignent un taux maximum en une semaine, puis diminuent et disparaissent en 3 à 6 mois.
Le taux des IgG s’élève rapidement, il est à son maximum après 60 jours suivant la contamination. Il diminue ensuite, mais persiste à un taux élevé pendant de longues années. Ce sont les IgG qui confèrent une immunité spécifique et durable. Le diagnostic repose sur la présence d’IgG et d’IgM dans le sérum, recherchées par des techniques ELISA. La présence associée d’IgM est la marque d’une infection récente, les IgG seules sont le reflet d’une infection ancienne.
Figure 1 : évolution des marqueurs au cours de l'hépatite A
2. Hépatite B
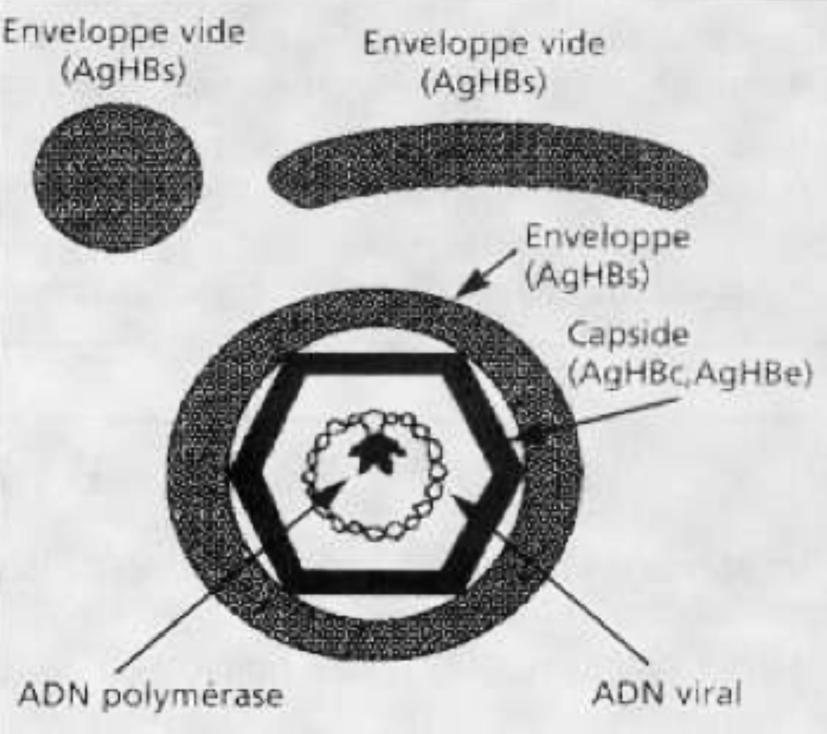
| Rappel sur le virus Si on examine au microscope électronique le sérum de patients en phase aiguë d'une hépatite à virus B, on observe différents types de particules : des particules sphériques de 42 nm de diamètre (particules virales complètes ou particules de Dan), des particules sphériques de 22 nm de diamètre et des bâtonnets. Les particules de 42 nm sont des particules virales infectieuses. Elles sont constituées d'une enveloppe sur laquelle les glycoprotéines virales portent un antigène de surface (AgHBs), d'une capside ou core portant un antigène de core (HBc) et d'un ADN. Les particules de 22 nm et les bâtonnets sont des enveloppes virales vides qui portent uniquement l'antigène HBs (figure 2). |
Figure 2 : virus de l'hépatite B, particules observées en microscopie électronique
Le diagnostic des différentes situations cliniques est effectué par la détection des marqueurs virologiques de l'infection. Il s'agit soit de méthodes immuno- enzymatiques de type ELISA, soit de techniques moléculaires détectant, quantifiant ou caractérisant la séquence de l'ADN du virus de l'hépatite B (VHB). Les éléments pouvant être mis en évidence dans le sérum sont soit des marqueurs directs de la présence virale, soit des marqueurs dits indirects liés à la réponse immunitaire.
a. Marqueurs directs
- L'antigène HBs associé aux enveloppes virales est aisément mis en évidence dans le sérum des patients par des techniques immuno-enzymatiques de type ELISA.
- L'antigène HBc n'est pas retrouvé tel quel dans le sérum.
- L’antigène HBe est une protéine soluble, dérivée de la protéine de capside qui est détectée dans le sérum en cas de multiplication virale, également par des techniques immuno-enzymatiques de type ELISA.
- L'ADN viral circulant associé aux particules virales infectieuses est mis en évidence par des techniques de biologie moléculaire (charge virale).
b. Marqueurs indirects
Ce sont les anticorps secrétés par le patient lorsqu'il rencontre les différents antigènes du virus B : l'anticorps anti-HBs, les anticorps anti-HBc IgG et anti-HBc IgM, et l'anticorps anti-Hbe. Ils sont eux aussi détectés par des méthodes immuno-enzymatiques de type ELISA.
Dans les pays en développement, l'AgHBs est souvent le seul marqueur recherché couramment pour le diagnostic des infections et le dépistage des échantillons de sang à éliminer en transfusion sanguine. Un sujet AgHBs positif est considéré comme infecté par le virus de l'hépatite B, et son sang comme potentiellement infectieux.
A côté des méthodes ELISA, adaptées aux grandes séries, des tests individuels ont été développés. Simples, ne nécessitant ni matériel particulier, ni électricité, ils reposent sur des méthodes d'agglutination, d'immunofiltration ou d'immunochromatographie. Un résultat positif est donné par un point ou un trait coloré ou une agglutination visible à l'œil nu. Ces réactifs sont adaptés aux structures ayant peu de moyens et/ou recevant un nombre réduit de prélèvements.
c. Evolution des marqueurs en fonction de la pathologie (figure3)
Hépatite B aiguë
Dans les formes symptomatiques (qui ne représentent que 10 % des cas), après une période d'incubation de 10 semaines en moyenne, suivie d'une phase pré-ictérique de 7 jours environ, survient la phase ictérique. Biologiquement, on observe alors une augmentation importante des transaminases sériques, qui peuvent atteindre entre 10 et 100 fois la limite supérieure de la normale.
Le taux de prothrombine est normal ou modérément abaissé, en tout cas toujours supérieur à 50 % en l'absence d'évolution sévère.
Des examens virologiques permettent d'affirmer le diagnostic d'hépatite aiguë B :
- L'antigène HBs (qui peut être détecté 3 semaines environ avant les signes cliniques) est présent dans le sérum, ainsi que les anticorps anti-HBc de type IgM (les plus précoces) présents à un titre élevé.
- Les anticorps anti-HBc de type IgM peuvent, dans certains cas, être seuls présents lorsque l'antigène HBs a déjà disparu du sérum. Ceci se produit dans 10 % des cas environ.
Figure 3 : évolution des marqueurs de l'infection par le virus de l'hépatite B
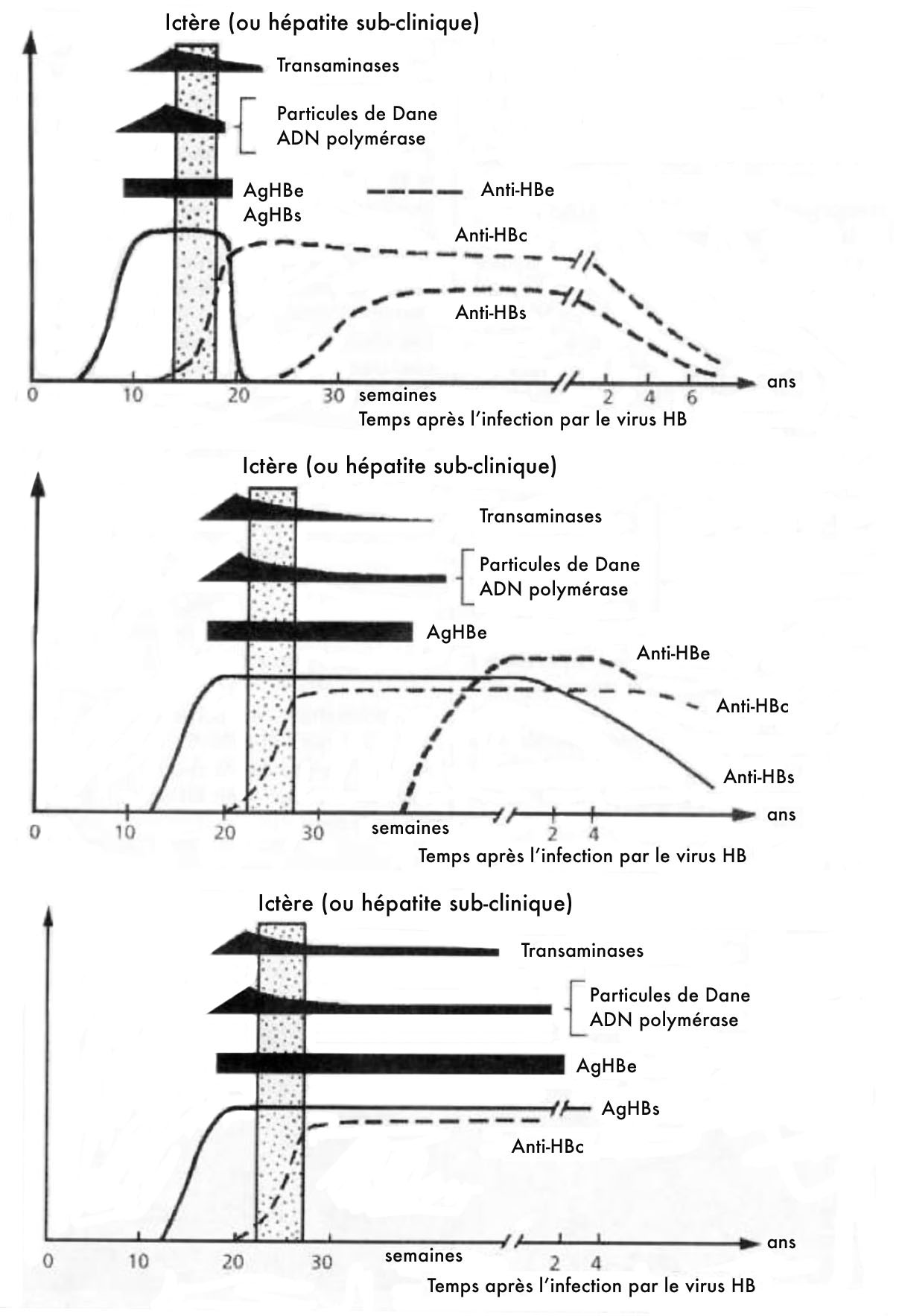
L'existence d'une augmentation des transaminases associée à un anticorps IgM anti-HBc permet de poser le diagnostic d'une hépatite B aiguë.
La détermination de l'antigène HBe et de l'anticorps anti-HBe ainsi que le dosage de l'ADN du virus de l'hépatite B ne sont pas utiles au stade d'hépatite B aiguë.
L'évolution est marquée dans plus de 90 % des cas par une disparition rapide de l'antigène HBs, puis par l'apparition d'anticorps anti-HBs neutralisants qui apportent une immunité définitive. Parallèlement, les transaminases sériques se normalisent.
Les anticorps anti-HBc de type IgM disparaissent et seuls vont persister les anticorps anti-HBc de type IgG et les anticorps anti-HBs.
Le taux de ces anticorps diminue lentement et, après de nombreuses années, il ne subsiste qu'un anticorps anti- HBs ou anti-HBc. Ce profil sérologique est celui d'une infection par le virus de l'hépatite B ancienne et guérie.
Hépatite aiguë sévère
Elle est caractérisée biologiquement par la diminution du taux de prothrombine (inférieur à 50 %) et doit conduire à une hospitalisation rapide en milieu spécialisé pour surveillance.
Hépatite fulminante
Elle survient dans 1 % des hépatites aiguës symptomatiques. Elle est toujours précédée d'une phase d'hépatite aiguë sévère. Elle est marquée biologiquement par un taux de prothrombine inférieur à 50% associé à une encéphalopathie hépatique.
Hépatite B chronique
Elle est définie par un portage d'antigène HBs d’une durée supérieure à 6 mois après l'épisode d'hépatite aiguë. L'infection se présente sous des formes variables, allant du portage asymptomatique de l'antigène HBs à l'hépatite chronique, la cirrhose, voire le carcinome hépato-cellulaire.
Portage asymptomatique
Un tiers des porteurs chroniques sont des porteurs asymptomatiques. Les transaminases sont normales. Il existe des anticorps sériques anti-HBe.
L'ADN viral est absent ou en quantité extrêmement faible, détectable uniquement par PCR. La surveillance de ces patients doit comporter annuellement le dosage des transaminases et la recherche des marqueurs de réplication virale : antigène HBe et anticorps anti-HBe (et ADN sérique si possible) pour surveiller une éventuelle reprise de la multiplication virale.
Hépatite chronique
Deux tiers des patients porteurs de l'antigène HBs vont développer des lésions d'hépatite chronique.
L'évolution se fait schématiquement selon 4 phases de durée variable.
- La première phase, qui dure de quelques mois à quelques années, est une phase de tolérance immunitaire. Elle est marquée par une multiplication active du virus avec un taux d'ADN sérique élevé et la présence d'antigène HBs dans le sérum.
- La deuxième phase est une phase d'immuno-élimination caractérisée par une flambée de la réponse immune, elle provoque la baisse de la multiplication virale et génère les lésions histologiques d'hépatite chronique. On observe une élévation transitoire, parfois très importante, des transaminases et la séroconversion antigène Hbe/anticorps anti-HBe, c'est-à-dire la diminution de l'antigène HBe jusqu'à sa disparition et l'apparition des anticorps anti-HBe.
- La troisième phase est une phase de portage inactif marquée par la quasi absence de marqueurs de la multiplication virale. L'antigène HBs a disparu, l'ADN sérique est très bas, et l'anticorps anti-HBe est présent.
- -La quatrième phase correspond à une élimination du virus qui devient indétectable.
Cependant, lorsqu'une cirrhose s'est développée, elle peut évoluer vers des complications et exposer le malade à la survenue d'un carcinome hépato-cellulaire.
Des épisodes de réactivation virale sont possibles, apparaissant soit spontanément, soit provoqués par des traitements immunosuppresseurs. Ils se traduisent par la réapparition des marqueurs de multiplication virale : antigène HBe et ADN sérique.
Carcinome hépato-cellulaire et dosage de l'alpha-fœtoprotéine
Sa fréquence élevée pourrait justifier une surveillance systématique des porteurs chroniques par dosage de l'alpha-fœtoprotéine sérique. C'est une glycoprotéine d'origine fœtale disparaissant pratiquement du sérum dans les semaines qui suivent la naissance. Son taux peut s'élever dans les hépatites aiguës et chroniques, les cirrhoses et surtout les cancers hépatiques.
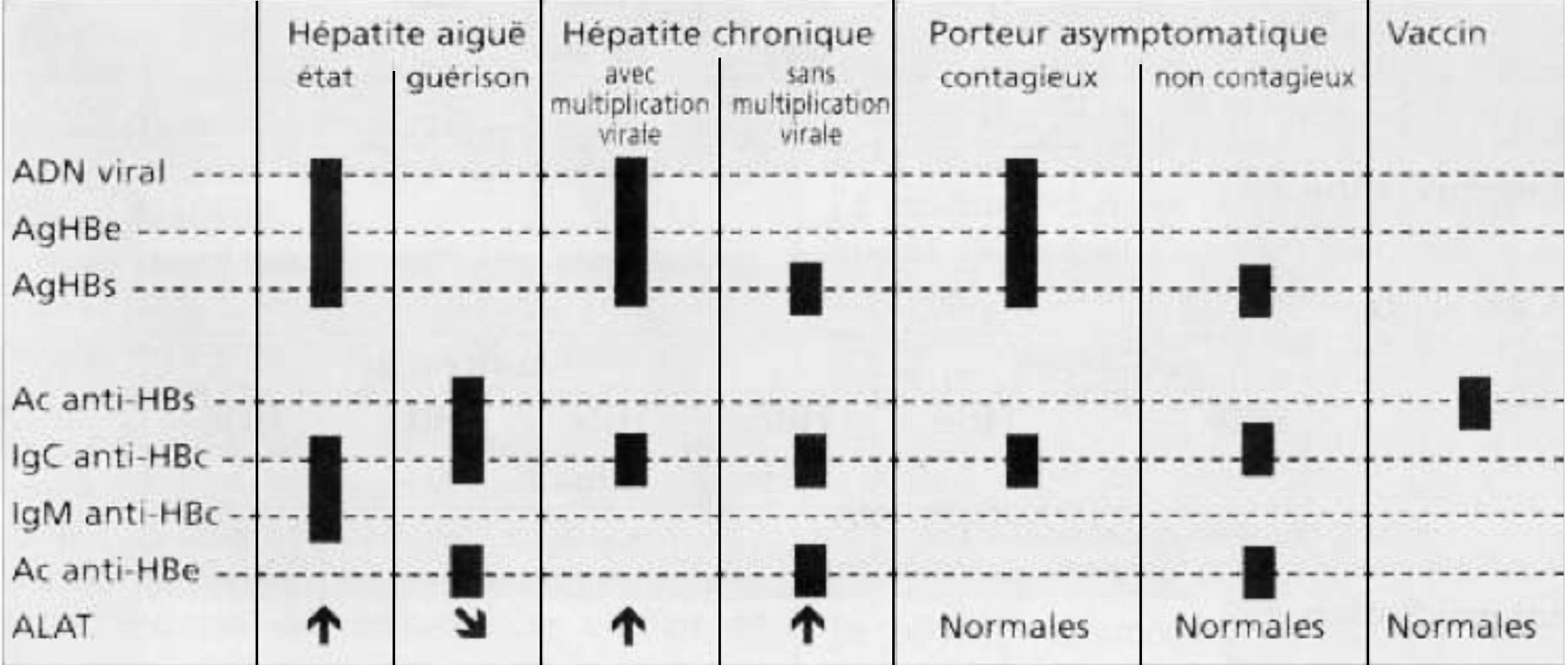
Les profils biologiques rencontrés lors d’une infection par le virus B sont résumés dans le tableau 1.
| AgHBs | AC anti-HBs | AC anti HBc | AgHBe | AC anti-HBe | ADN VHB | ||
| Ig totaux | IgM | ||||||
| Hépatite aiguë Hépatite aiguë (convalescence) | \+ \+ \- | \- \- \- | \+ \+ \+ | \+ \+ \+ | \+ \- \- | \- \+ \+ | \+ \- \- |
| Hépatite ancienne guérie | \- \- | \+ \- | \+ \+ | \- \- | \- \- | +/- +/- | \- \- |
| Vaccination | - | + | - | - | - | - | - |
| Hépatite chronique à IT IE Réactivation | \+ + + | \- - - | \+ + + | \- +/- +/- | \+ +>- + | \- +>- - | \- +/- +/- |
| Cas particuliers |
|---|
| Mutants pré-core Caractérisés par l’absence de production d’AgHBe, on les observe en phase chronique, à la suite de la sélection naturelle d’un variant pré-core. Les anticorps antiHbe sont présents, ils ont été produits au moment où l’antigène dit sauvage était encore présent. L’absence d’AgHbe ne signifie pas forcément une absence de réplication, c’est la mesure de la charge virale qui permet de différencier un portage chronique sans réplication virale d’une infection chronique par un virus mutant pré-core qui se réplique. Mutants “S” Du fait d’une mutation dans le gène S ou dans le gène pol du VHB, les tests habituels pour la détection de l’AgHBs peuvent être faussement négatifs. La détection de l’ADN viral doit être alors effectuée. Hépatite B occulte Malgré l‘absence d’AgHBs dans le sérum, il persiste une réplication virale faible. Là aussi, la détection de l’ADN viral doit être effectuée. La fréquence de l’infection occulte par le VHB est de 5 à 10 % chez les patients infectés par le VIH. |
d. Contrôle de l'immunité
La recherche et le dosage des anticorps anti-HBs renseignent sur le niveau d'immunité du patient.
Avant vaccination
On recherche les anticorps anti-HBc totaux et les anticorps anti-HBs. Ce dépistage est utilisé dans les groupes à risque pour éviter de vacciner un sujet guéri
ou ayant une hépatite chronique.
Après vaccination
Il s'agit du titrage des anticorps anti-HBs, seul marqueur présent chez un sujet vacciné. En effet l'administration du vaccin anti-hépatite B, constitué d'antigène HBs recombinant, induit la production d'anticorps anti-HBs neutralisants protecteurs mais pas la production d'anticorps anti-HBc. Le seuil de protection a été fixé par l'OMS à 10 mUl/mL. Un titre supérieur, de 30 à 50 mUl/mL, semble toutefois assurer une meilleure protection. Le contrôle du titre des anticorps anti-HBs après vaccination n'est pas systématique et doit être réservé aux sujets à risque d'infection qui doivent savoir dans quelle mesure ils sont protégés.
La découverte d'une hépatite B aiguë ou chronique chez un sujet doit conduire à la vérification de l'immunisation des sujets contact par la recherche, chez le ou les partenaires sexuels et chez les membres de la famille, de l'antigène HBs et de l'anticorps anti-HBs. Les sujets non immunisés doivent bénéficier d'une immunoprophylaxie (au moins par la vaccination).
Autres marqueurs virologiques
Compte tenu des modes de contamination communs, il est recommandé, chez un patient porteur du virus de l'hépatite B, de rechercher une infection associée par le virus de l'hépatite C et de conseiller un dépistage du virus de l'immunodéficience humaine.
Transfusion sanguine
La recherche des marqueurs des hépatites B et C est obligatoire pour tous les produits (PSL) destinés à la transfusion sanguine. Selon les pays, elle s’effectue par biologie moléculaire ou, en l’absence de ces techniques, par la recherche de l'antigène HBs et de l'anticorps anti-HBc total, ainsi que le dosage des transaminases.
| Les déterminations de l'antigène HBs, de l'anticorps anti-HBc et de l'anticorps anti-HBs permettent le diagnostic de l'hépatite B aiguë. Les déterminations de l'antigène HBs, de l'antigène HBe et de l'anticorps anti-HBe sont nécessaires au suivi de l'hépatite chronique B. |
3. Hépatite Delta
Il peut s’agir d’une infection concomitante par le VHB et le VHD, ou d’une surinfection par le VHD au cours d’une hépatite B chronique.
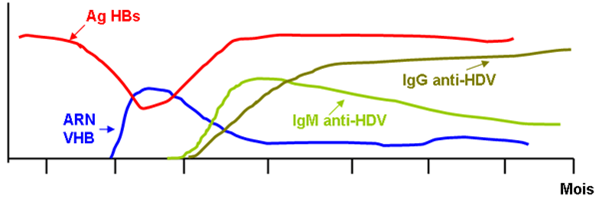
Le diagnostic se fait par recherche des anticorps totaux anti-VHD et des IgM ; il doit être complété par une recherche d’ARN-VHD qui ne se fait qu’en laboratoire spécialisé (voir figure 5).
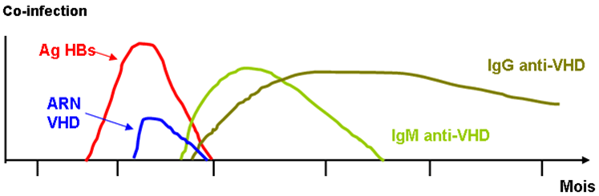
Surinfection
4. Hépatite C
Le diagnostic se fait par technique ELISA au moyen de tests plus performants dits tests de 3ème génération. Deux tests différents doivent être effectués, pour le dépistage et la confirmation. La détection des anticorps anti VHC n’est positive que 12 à 15 semaines après la contamination, et l’on n’est pas encore en mesure de distinguer IgM et IgG.
Des tests rapides d’orientation diagnostique (TROD) ont été récemment évalués : mise en évidence des anticorps anti-VHC en 10 minutes sur une goutte de sang prélevée au bout du doigt :
- si la réponse est négative, le patient n’a pas contracté le VHC,
- si le test est positif, une prise de sang devra être effectuée pour confirmation.
Ces tests seraient d’un grand intérêt dans le dépistage de masse. La détection du portage chronique se fait par la mesure de l’ARN viral dans le sérum.
Indications de la mesure de la charge virale :
- Sérologie VHC positive
- Sérologie VHC douteuse
- Sujet VIH positif fortement immunodéprimé
- Début de traitement anti VHC
- En cours de traitement
- En fin de traitement
- Six mois après l’arrêt du traitement.
5. Hépatite E
Les anticorps anti-VHE de type IgM et IgG sont détectés dès l’apparition des symptômes, leur taux est au maximum après un mois. Les IgM disparaissent en 2 à 6 mois. Les IgG persistent de 18 mois à plus de 10 ans. Des cas d’hépatite chronique et de cirrhose ont été observés chez des patients immunodéprimés, chez qui la mesure de l’ARN-VHE a été effectuée.
L’hépatite fulminante est fréquente chez la femme enceinte et en cas d’immunodépression.
Le nombre de particules virales est exprimé en puissance de 10 ou en échelle logarithmique
|
6. Autres virus
D’autres virus peuvent être responsables d’une hépatite associée à d’autres signes cliniques et biologiques :
- Au cours des arboviroses (dengue, fièvre jaune, Chikungunya).
- Au cours de la mononucléose infectieuse, des infections à CMV : dans ces cas, l’hépatite est le plus souvent bénigne ou asymptomatique.
Conclusion
Le suivi biologique des hépatites est d'une grande aide pour le clinicien. Les transaminases et le taux de prothrombine sont des marqueurs essentiels qui apprécient la gravité de l'atteinte hépatique et la notion de l'urgence dans les cas d'hépatites sévères. Ils sont accessibles aux laboratoires de routine. L'étude des marqueurs virologiques nécessite l'emploi de réactifs commercialisés de coût non négligeable, l’intervention de techniciens bien entraînés car il s'agit de manipulations délicates, et une
bonne interprétation. Les techniques de biologie moléculaire, délicates et d'un coût important, restent pour l'instant effectuées dans les laboratoires spécialisés.